La ciencia consigue producir hidrógeno verde con luz en lugar de electricidad
Son numerosas las empresas que están apostando por el hidrógeno verde como fuente de energía sostenible. Sin embargo, el proceso de obtención del mismo es aún complejo y costoso. Por eso, el hallazgo de estos científicos austriacos puede ser vital para el futuro.

El hidrógeno verde está en plena expansión y, especialmente tras la invasión rusa a Ucrania y la consiguiente crisis energética surgida de dicho conflicto, esta fuente de energía sostenible ha sido una de las que más impulso ha obtenido.
Pero el hidrógeno verde plantea, de momento, muchas complejidades que limitan su democratización. Una de las principales es que es complejo de obtener, pues el proceso de electrólisis es caro y requiere de maquinaria y materiales costosos.
«No queremos simplemente confiar en un enfoque de prueba y error, queremos descubrir a nivel atómico cuál es realmente el catalizador óptimo»»
No son pocos los proyectos que buscan solucionar este problema. Por ejemplo, con la obtención de catalizadores no metálicos o hacer uso de nuevas fuentes para producir hidrógeno, como las microalgas con las que trabajan estos científicos israelíes.
Luz en lugar de electricidad
Pues bien, los investigadores austriacos de la Universidad Técnica de Viena (TU Wien) están experimentando con la luz como detonante del proceso de electrólisis, que en la actualidad se realiza siempre con la intervención de la electricidad.
El proceso de electrólisis es el siguiente: se aplica electricidad al agua mediante un electrolizador provisto de catalizadores, es decir, un ánodo y un cátodo. De este modo, se separan las moléculas de oxígeno de las de hidrógeno. Para obtener hidrógeno verde, la electricidad debe provenir de energías renovables, generalmente solar y eólica.
Pero, ¿y si no fuera necesaria la intervención de la electricidad, sino simplemente la luz? Esto es lo que han conseguido los científicos en un proceso que denominan división fotocatalítica del agua.
Según Alexey Cherevan, del Instituto de Química de Materiales de TU Wien, «en realidad, para poder dividir el agua con la luz, es necesario resolver dos tareas al mismo tiempo. Tenemos que pensar en el oxígeno y en el hidrógeno. Los átomos de de oxígeno del agua deben transformarse en moléculas de O2; y los iones de hidrógeno restantes, que sólo son protones, deben convertirse en moléculas de H2».
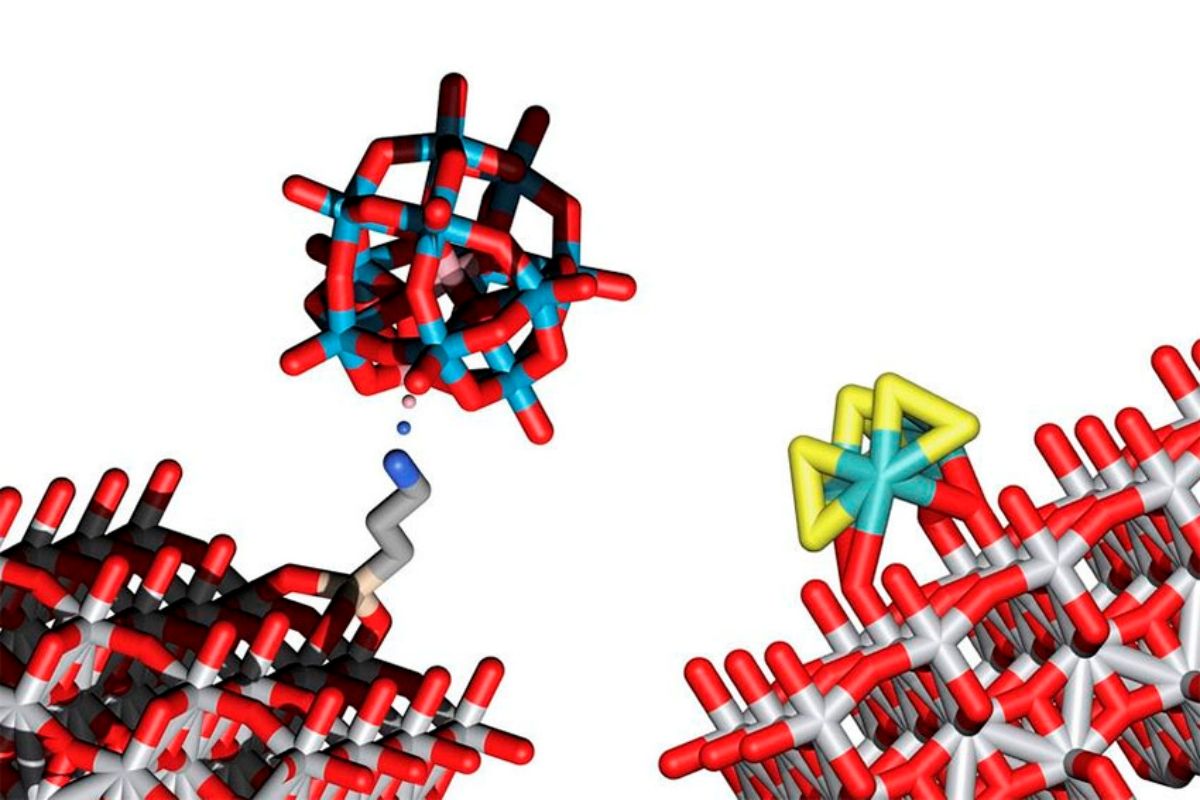
Para solucionar este problema, los científicos han utilizado pequeños grupos inorgánicos formados por una pequeña cantidad de átomos anclados en una superficie de estructuras de soporte que absorben la luz, como es el caso del óxido de titanio. La combinación de conjuntos de átomos y soportes de semiconductores cuidadosamente elegidos hace posible el comportamiento deseado.
Para formar los conjuntos de átomos responsables de oxidar el oxígeno se han utilizado cobalto, tungsteno y oxígeno. Por su parte, el azufre y el molibdeno son adecuados para crear moléculas de hidrógeno. Posteriormente, estos grupos se depositan en una superficie hecha de óxido de titanio».
Una superficie y luz del sol
Con el sistema actual de electrólisis, es necesaria la intervención de una fuente de energía sostenible, células fotovoltaicas o aerogeneradores y dispositivos de almacenamiento de energía eléctrica, además de un electrolizador.
Sin embargo, con este sistema lo único que hace falta es una superficie adecuadamente recubierta sumergida en agua y radiación solar.
«El óxido de titanio es sensible a la luz, eso ya se sabía. La energía de la luz absorbida conduce a la creación de electrones de libre movimiento y cargas positivas de libre movimiento en el óxido de titanio. Estas cargas permiten que los grupos de átomos que se encuentran en esta superficie faciliten la división en oxígeno e hidrógeno», amplía Cherevan.
«Para dividir el agua con luz, los científicos se basan en nanopartículas que pueden adoptar formas y propiedades superficiales muy diferentes. Los tamaños son difíciles de controlar, los átomos no están dispuestos de la misma manera. Por lo tanto, en este caso, no es posible explicar exactamente cómo se lleva a cabo el proceso de catálisis en detalle».
Por tanto, el siguiente paso es encontrar el catalizador óptimo para conseguir la mayor eficiencia posible en el proceso. «No queremos simplemente confiar en un enfoque de prueba y error y probar diferentes nanopartículas hasta que encontremos la mejor. Queremos descubrir a nivel atómico cuál es realmente el catalizador óptimo», afirma Cherevan.
«La ventaja decisiva de nuestro método sobre la división del agua por electrólisis es su simplicidad», finaliza.
Fuente: Energy News

